A bioimpressão é a impressão de células e tecidos vivos. É uma técnica promissora que, com sorte, um dia poderá resolver a escassez de doadores de órgãos, cultivando órgãos a partir das próprias células dos pacientes. No entanto, imprimir tecidos e células vivas é extremamente complicado e muitos obstáculos precisam ser superados para chegar lá. Neste artigo, são destacadas três soluções de bioimpressão volumétrica recentemente desenvolvidas pela UMC Utrecht que ajudarão a tornar a bioimpressão mais clinicamente relevante.
Aumento da bioimpressão volumétrica
A primeira associação com a bioimpressão 3D é a impressão 3D ‘clássica’ ou impressão por extrusão com filamento de plástico. Isso se tornou popular nos últimos 15 anos, à medida que as impressoras de baixo custo se tornaram amplamente disponíveis. Em princípio, deveria ser possível substituir o plástico e imprimir pedaços de tecido biologicamente funcional, com diferentes tipos de células presentes. Mas para conseguir isso, tecidos altamente detalhados e diferenciados terão que ser feitos: mesmo um milímetro cúbico de tecido de órgão também precisará de capilares sanguíneos, então a fasquia é muito alta para impressoras se quisermos criar tecido funcional que nós pode implantar em uma escala clinicamente relevante.

Com o desenvolvimento das biotintas, a bioimpressão por extrusão 3D tornou-se possível. Novos bicos, tintas nutritivas e andaimes pré-fabricados tornam mais fácil para as células sobreviverem a esse processo. E usando várias tintas ao mesmo tempo, diferentes tipos de células podem ser depositados e, assim, criar tecidos. No entanto, a impressão camada por camada ainda leva muito tempo; muitas horas para um objeto de vários centímetros cúbicos. As células provavelmente morrerão durante esse processo. Além disso, as impressões de extrusão precisam resistir à gravidade, portanto, as tintas precisam ser resistentes, o que significa que não são muito compatíveis com as células.
Para superar esse processo lento e dependente da gravidade, a impressão volumétrica também foi adotada para bioimpressão. Nesse processo, um frasco giratório com um gel especial é exposto à luz do laser. Onde a luz do laser atinge, o gel fotossensível se solidifica rapidamente. Isso significa que, com uma reconstrução de luz 3D a laser, formas intrincadas de vários centímetros cúbicos podem ser criadas em questão de segundos. Agora, enquanto isso resolve o problema de velocidade e gravidade, ele vem com suas próprias desvantagens.
Esses géis fotossensíveis podem, dessa forma, conter apenas células em suspensão, portanto, controlar que tipo de célula vai parar onde – e quantas delas – é difícil de controlar. E como o gel é duro, é difícil que as células se movam, se estendam e se comuniquem, o que é essencial para a formação ou mesmo para o funcionamento do tecido.
No Centro de Medicina Regenerativa de Utrecht, os pesquisadores trabalham continuamente para superar esses desafios, e os três artigos discutidos abaixo resolveram parte dos desafios descritos acima.

Criando regiões biologicamente funcionais em uma impressão
A bioimpressão volumétrica, com a qual um objeto de alguns centímetros pode ser impresso em poucos segundos, oferece muitas possibilidades para a impressão de células. A velocidade do processo combinada com a compatibilidade celular do gel são grandes vantagens. No entanto, quando a impressão é concluída, as células podem não ser colocadas exatamente onde são necessárias, nem é possível alterar muito o gel para auxiliar no desenvolvimento, crescimento ou especialização das células para criar tecidos funcionais. Superar esse obstáculo, então, é importante, porque em nosso corpo as células sabem para onde ir e onde ficar seguindo sinais que sentem em regiões ou tecidos específicos.
Adicionando funcionalidade ao gel impresso
Para possibilitar alterações químicas na impressão após o processo inicial de impressão, os pesquisadores brincaram com a porosidade do gel, bem como com os compostos que se ligam a outras moléculas do gel. “Com esta técnica, é possível enxertar biomoléculas em nossas construções impressas em minutos em alta resolução espacial”, explica o primeiro autor Marc Falandt. “Primeiro, imprimimos nossas construções baseadas em gelatina com a impressora volumétrica e, em seguida, infundindo essas construções com biomoléculas e fotoiniciador, poderíamos criar motivos 3D complexos dentro das estruturas de gelatina. Esse método nos dá controle tridimensional do local onde você deseja que suas biomoléculas fiquem presas. Algo que antes não era possível.”
Ajudar as células a encontrar seu caminho, fornecendo-lhes um mapa químico
Com esta inovação, agora é possível criar impressões volumétricas que podem ter fatores de crescimento ou proteínas bioativas “pintadas” em qualquer formato 3D desejado. Por exemplo, moléculas sinalizadoras que orientam a direção e a formação de vasos sanguíneos podem ser colocadas de forma a criar um rastro que atrai novos vasos somente onde e quando necessário dentro do objeto impresso em 3D.
Esses sinais poderiam atrair as células certas ou ajudar as células-tronco a cumprir seu potencial regenerativo. Falandt: “Este trabalho realmente dá os primeiros passos no desenvolvimento e caracterização de materiais inteligentes que permitem a edição bioquímica em 3D. Em combinação com a técnica de bioimpressão volumétrica rápida, esta abordagem é extremamente promissora para a criação de andaimes biofabricados que podem orientar o comportamento e o desenvolvimento das células. Isso poderia nos permitir imitar de perto o complexo ambiente bioquímico de tecidos e órgãos nativos com nossas bioimpressões 3D.
Géis granulares para células impressas
Para um tecido fabricado com sucesso, as células impressas precisam ser mimadas para sobreviver e prosperar no produto acabado. E para formar um tecido funcional, eles precisam ser capazes de crescer, se mover e se comunicar uns com os outros.
Várias estratégias de impressão foram tentadas para resolver isso, e todas elas têm seus prós e contras. Na impressão por extrusão 3D, as células podem ser depositadas em uma variedade de tipos e com números elevados, mas esse processo é muito demorado, causa estresse mecânico às células e é dependente da gravidade – tudo prejudicial à sobrevivência e ao funcionamento das células. Com a bioimpressão volumétrica rápida, a velocidade e a gravidade podem ter sido resolvidas, mas aqui o desafio é que as células são distribuídas aleatoriamente na resina e em números menores e, como a impressão final consiste em resina sólida, as células não conseguem funcionar e se comunicar adequadamente .
Criando um micromundo granular
Para resolver esse problema, os materiais utilizados para a bioimpressão devem fornecer um ambiente que permita a auto-organização e a comunicação das células. Embora isso geralmente seja possível com hidrogéis macios, garantir alta resolução de impressão e fidelidade de forma desses materiais continua sendo um gargalo importante, especialmente ao usar técnicas convencionais de fabricação de camada por camada.
O primeiro autor Davide Ribezzi explorou o uso de resinas granulares para superar esses desafios. “Os géis granulares são basicamente micropartículas de gel compactadas juntas”, disse Ribezzi. “Embora cada micropartícula possua propriedades comparáveis à sua contraparte de hidrogel a granel, as partículas de microgel empacotadas podem ser projetadas e personalizadas para exibir uma ampla gama de propriedades úteis adicionais”. Aproveitar os biomateriais particulados é, portanto, uma estratégia promissora para enfrentar as desvantagens relacionadas ao encapsulamento de células a granel e à processabilidade do material nos processos de impressão.
Combinando diferentes estratégias de impressão
As resinas granuladas de fato permitiram aos pesquisadores combinar extrusão e impressão volumétrica. Usando a impressão por extrusão, certas células ou outros produtos químicos podem ser especificamente depositados na resina. Essa abordagem otimiza o equilíbrio entre a velocidade da impressão volumétrica com a precisão da impressão por extrusão. O gel se move ao redor do bocal de impressão como creme ao redor de um dedo intrusivo, de modo que as células podem ser colocadas em várias camadas rapidamente, sem ter que se preocupar com a resistência da estrutura. Em seguida, a impressão volumétrica pode finalizar o processo criando e aprimorando as formas ao redor das células extrudadas.
Este processo teve seus desafios. Ribezzi: “Processar materiais biológicos sempre requer muita atenção e planejamento meticuloso dos experimentos. Mas em nossa pesquisa, exploramos as propriedades térmicas do microgel, o que permite o ajuste preciso das propriedades mecânicas e ópticas. Isso se traduziu em estímulos sintonizáveis detectados pelas células incorporadas. No entanto, esse grau mais alto de afinação exigia um grau ainda maior de atenção e precisão durante o processo de impressão.”
Mais atividade biológica
Experimentos com células confirmam que as resinas granuladas permitem muito mais atividade biológica após a impressão, superando amplamente os géis sólidos. Oito dias após serem impressas na resina, as células-tronco foram capazes de se espalhar mais, as células endoteliais criaram mais junções e as células semelhantes a neurônios fizeram mais conexões umas com as outras.
Ribezzi comentou ainda: “Para estudos futuros, prevemos a mistura e até a padronização local de microgéis obtidos de diferentes materiais. Isso nos permitiria criar construções compostas com propriedades únicas ou com bolsos bioativos liberando, por exemplo, drogas. Essas ferramentas aumentarão a funcionalidade do tecido e abrirão oportunidades adicionais para engenharia de tecidos, medicina regenerativa e a área emergente de materiais vivos projetados”.
Técnicas de bioimpressão para vasos sanguíneos funcionais
A bioimpressão volumétrica é uma técnica rápida, que permite que as células sobrevivam ao processo de impressão. No entanto, como esse tipo de impressão é feito em géis compatíveis com células, as impressões resultantes não são estruturalmente muito sólidas. Este é um problema para os vasos sanguíneos impressos, que devem ser capazes de suportar altas pressões e flexões. Por esta razão, uma fusão de bioimpressão volumétrica e eletroescrita fundida foi buscada.
A eletroescrita por fusão é um tipo altamente preciso de impressão 3D que funciona direcionando um filamento estreito de plástico fundido (biodegradável). É capaz de produzir andaimes intrincados que são mecanicamente fortes e capazes de lidar com a força. A desvantagem aqui é que eles não podem ser impressos com células diretamente, por causa das altas temperaturas envolvidas. Portanto, a bioimpressão volumétrica foi usada aqui para solidificar géis carregados de células nos andaimes.
Mesclando eletroescrita e impressão volumétrica
O processo começa com a criação de um andaime tubular usando eletroescrita derretida. Este é então submerso em um frasco com gel fotoativo e colocado na bioimpressora volumétrica. Em princípio, o laser da impressora pode solidificar seletivamente o gel que fica dentro, sobre e/ou ao redor do andaime. “Para acertar, tivemos que colocar o andaime exatamente no centro do frasco”, disse o primeiro autor Gabriël Größbacher. “Qualquer desvio do centro significaria que a impressão volumétrica seria deslocada. Mas conseguimos centralizá-lo perfeitamente imprimindo o andaime em um mandril que encaixamos no frasco.”
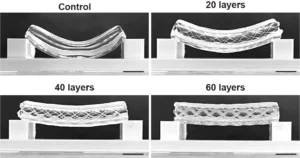
Neste estudo, Größbacher e colegas testaram várias espessuras do andaime, o que resultou em tubos mais ou menos fortes. Por fim, eles também testaram várias colocações dos géis bioimpressos. Estes podem ser colocados no lado interno do andaime, dentro do próprio andaime ou fora dele. Usando duas células-tronco marcadas de forma diferente, a equipe conseguiu imprimir uma prova do princípio do vaso sanguíneo com duas camadas de células-tronco e células epiteliais semeadas no centro para cobrir o lúmen do vaso.
De tubos a vasos funcionais
O desenho também poderia permitir furos na lateral da impressão, dando a possibilidade de permeabilidade controlada do vaso para que o sangue faça sua função. Por fim, os pesquisadores também criaram estruturas mais complexas, como vasos bifurcados e até mesmo vasos com válvulas venosas que funcionavam na manutenção de um fluxo unidirecional.
Größbacher: “Esta foi uma prova de estudo de princípio. O que precisamos fazer agora é substituir as células-tronco por células funcionais que fazem parte de um vaso sanguíneo real. Isso significa adicionar células musculares e tecido fibroso ao redor das células epiteliais. Nosso objetivo agora é imprimir um vaso sanguíneo funcional.”
Embora essas inovações ofereçam opções interessantes para levar adiante a bioimpressão, ela funcionará melhor se elas puderem ser combinadas e expandidas. O líder do grupo, Riccardo Levato, afirmou: “Ser capaz de imprimir moléculas biologicamente ativas em uma impressão que usa gel granular significa que as células podem usar melhor as informações moleculares, além de crescer e se desenvolver em um tecido, juntamente com as células vizinhas”. Para saber mais acesse o site.


